随着社会的发展和科技的进步,人类物质生活水平不断提高,肥胖在过去数十年内呈现全球范围的流行并严重影响人类健康。2017年NCD-RisC组织(非传染性疾病风险控制协作组织)在《柳叶刀》杂志上发布了全球肥胖数据的调查结果,显示40年内全球成人肥胖人数从约1亿飙升至6.5亿。
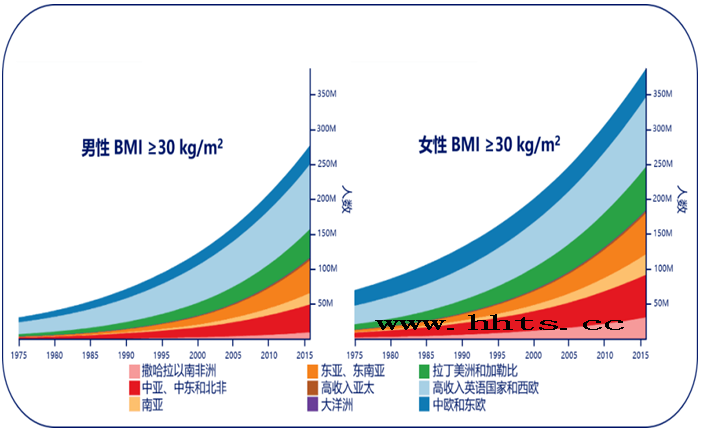
图1表示横跨40年肥胖与核心病症发病联系
随着对肥胖了解的深化和发展,人们认识到肥胖不仅仅是体重增加,还会同时伴有一系列慢性并发疾病组成的症候群,包括2型糖尿病、高血压、睡眠呼吸暂停、多囊卵巢综合征等。这些以肥胖为核心的病症群与心血管病的发病联系亦日渐明确。一项横跨40年随访时间(1964-2015)、汇总10个美国大型前瞻性队列研究的流行病学研究数据显示,随着体重指数的增加,心血管事件的风险显著增加。所以我们可能就会想到一些问题,肥胖为什么会增加心血管疾病风险?减重治疗对心血管疾病有什么影响?减重药物对心血管结局有什么影响?本期我们就带着以上三个问题,从由肥胖带来的千钧重负与相关心血管结局的各项研究中寻找结果。肥胖对心血管疾病风险的影响:首先,既往研究显示,肥胖是公认的动脉粥样硬化、缺血性心脏病、充血性心力衰竭和卒中等疾病的危险因素。但是我们不能将肥胖当作单个疾病来看,多项研究发现,肥胖可以导致200多种并发症。其中许多并发症如2型糖尿病、非酒精性脂肪肝、睡眠呼吸暂停等也是心血管疾病(CVD)的危险因素4,5。可见,肥胖增加心血管疾病风险的部分原因很可能是叠加在多项并发症之上的。那么,单纯的肥胖是否也会增加心血管疾病风险呢?来自英国伯明翰大学的学者Rishi Caleyachet对此进行了一项队列研究。他将1995年至2015年数据库收集到的350万无心血管疾病人群,按照BMI和三种代谢异常(糖尿病、高血压和高脂血症)进行分类,在平均5.4年的随访时间中,观察记录他们的心血管事件。结果发现,即使没有以上三种代谢异常,超重和肥胖也会增加心血管疾病的风险(图2)。
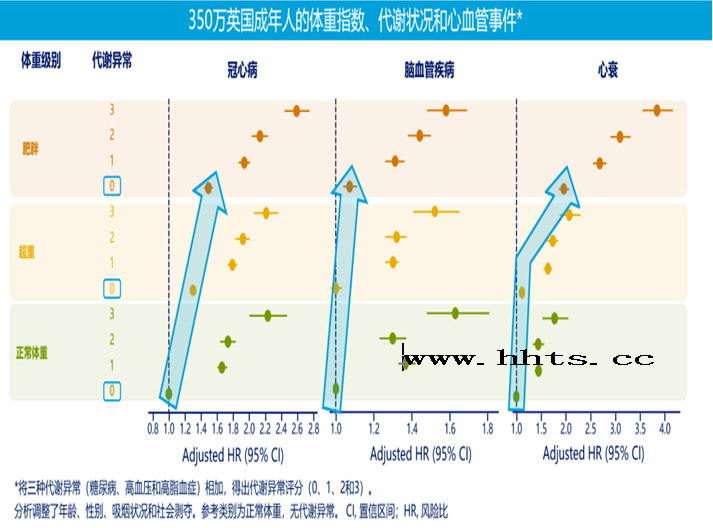
图2表示没有代谢异常
超重和肥胖也会增加心血管疾病的风险。那么,肥胖又是从哪些病理生理机制,导致心血管疾病风险的增加呢?肥胖的核心表现之一,就是脂肪的积聚。除了血脂的增加外,由脂肪异常沉积还会引起包括血压升高、血糖升高、胰岛素抵抗及各种异常的炎症因子增加等在内的病理生理改变。以上改变从各个方向促进血管表面的黏附分子表达、泡沫细胞形成、平滑肌增殖及脂质和胆固醇沉积,促进了斑块的形成,进一步改变了动脉的血流动力学。失去弹性的血管和不定时脱落的斑块随时都可能“引爆”心血管事件的发生。同时,异常的脂肪聚集还会通过促进2型糖尿病、非酒精性脂肪肝及肝硬化等进一步增加心血管事件的发生风险(图3)。
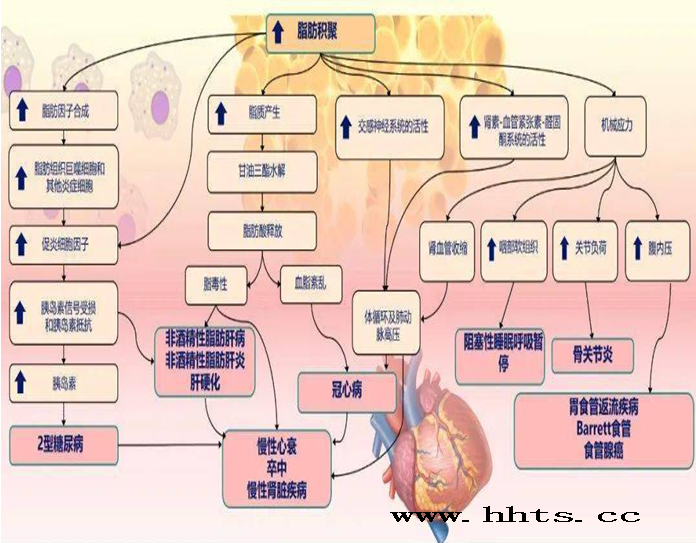
图3表示 肥胖致心血管疾病及相关慢性疾病的关键机制
减重治疗对心血管疾病风险因素和结局的影响:从以上的病理生理改变出发,我们再来聊聊减重对心血管疾病风险的影响。既往的多项研究显示,减重治疗能够带来血压/血脂/血糖降低、改善胰岛素抵抗、降低炎症因子水平等诸多获益,进而降低心血管疾病的发生风险 9,10,11。目前,最常见的减重治疗方式包括生活方式干预、代谢手术和药物治疗(图4)。就减重效果而言,生活方式干预<药物治疗<代谢手术。那么它们对心血管疾病的结局影响是一样的吗?
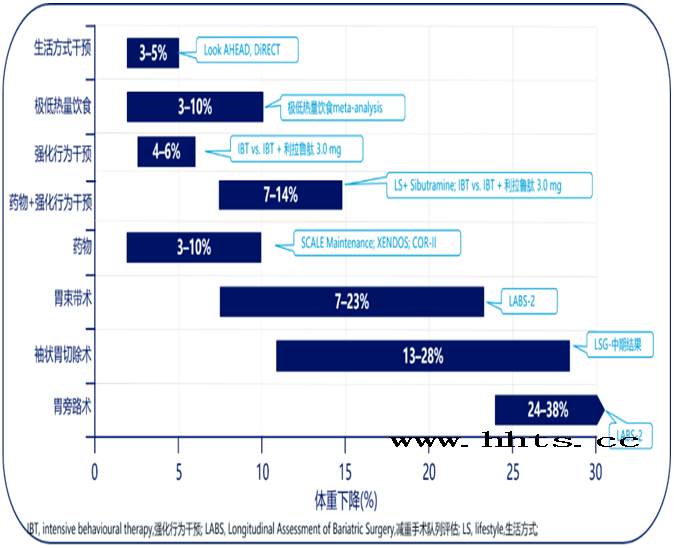
图4表示目前减重干预措施的各项研究及其疗效结果汇总
生活方式干预:最为经典的莫过于由美国国立卫生研究院资助的LookAHEAD研究。该研究是一项前瞻性、多中心、随机对照临床研究,旨在评估超重或肥胖2型糖尿病患者采用强化生活方式干预减轻体重能否减少心血管事件和死亡。最终的结果提示,在超重或肥胖的成人2型糖尿病患者中,以减轻体重为主要目标的强化生活方式干预并不能降低心血管事件的发生率。进一步的事后分析显示,仅在体重减轻≥10%的患者中发现了MACE风险的显著降低(图5)。
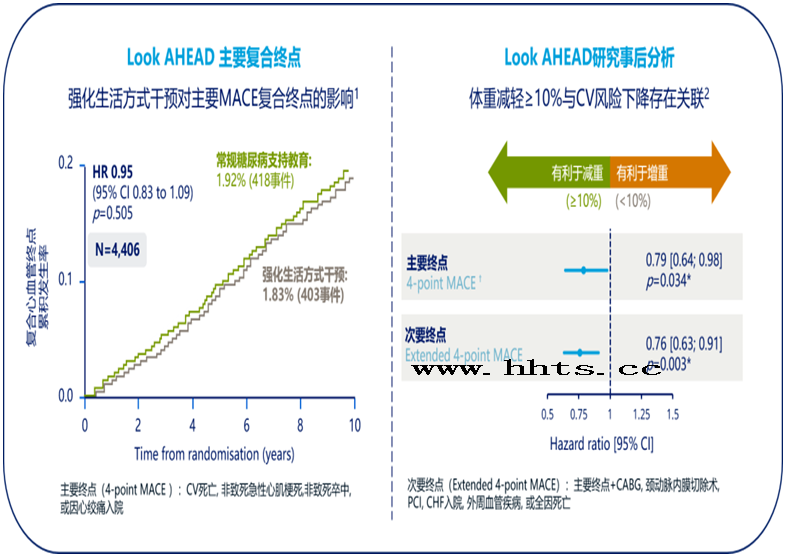
图5表示 Look AHEAD研究及其事后分析
在超重/肥胖合并2型糖尿病的患者中,仅在体重减轻≥10%的患者中发现了MACE风险的显著降低。中国的大庆研究评估了6年的生活方式干预试验(饮食±运动)对糖耐量受损人群的长期影响,纳入人群的平均BMI为25.7 kg/m 2 (仅在BMI>25 kg/m 2 的人群中鼓励减重)。在大庆研究后续30年的随访中,与对照组相比,生活方式干预组的心血管事件累积发生率降低26%,其中卒中发生率降低25%,冠心病发生率降低27%,心力衰竭发生率降低29%。可见,在肥胖/超重合并2型糖尿病/糖耐量异常的人群中,生活方式干预能够一定程度上降低心血管疾病的发生风险。代谢手术:对于生活方式干预和药物治疗均不能控制的肥胖患者(尤其是BMI>40 kg/m 2 ),代谢手术是目前最有效的治疗手段。那么代谢手术会改变患者的心血管疾病结局吗?瑞典肥胖受试者(SOS)研究比较了经常规治疗或减重手术的两组肥胖患者人群的差异。经过中位时间为14.7年的随访,结果显示,与未接受手术相比,减重手术显著降低心血管死亡风险53%(p=0.002)和心肌梗死或卒中风险33%(p<0.001)。另一项平均随访7.1年的回顾性队列研究表明:在肥胖患者人群中,减重手术较之于非手术治疗,降低了合并冠心病患者死亡率风险56%,降低合并2型糖尿病患者死亡风险达92%。减重药物:药物治疗既有比生活方式干预更强的减重疗效,又没有手术治疗附带的对身体的创伤,因此一直在肥胖治疗中有很高的呼声。与之相对的则是在百余年的发展史中,多种减重药物因严重并发症纷纷退场。目前减重药物只能作为生活方式治疗的辅助手段,不建议单独使用。现有的减重药物主要通过调节中枢食欲或/和调控外周的消化吸收起效(图6),它们的疗效都有相应的临床试验结果,但是它们对心血管疾病的发生风险有什么影响呢?带着以上问题我们将引入CVOT研究对减重药物研发历程的重要改变。
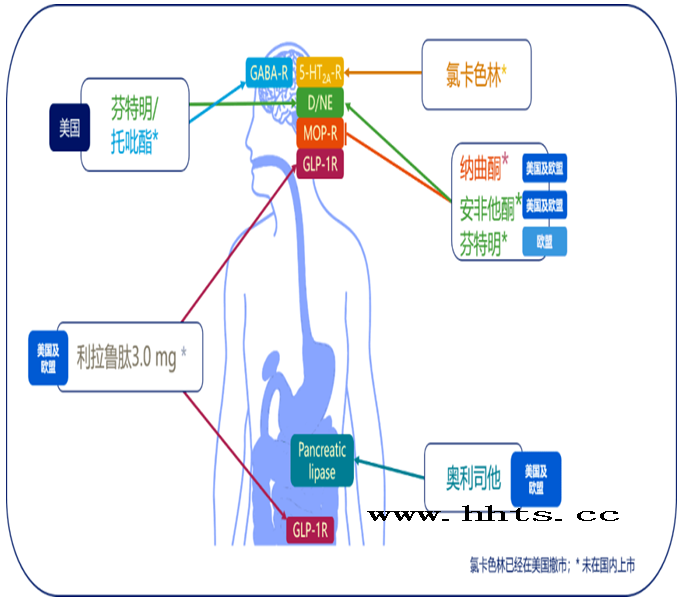
图6表示减重药物及其作用靶点
减重药物对心血管结局的研究:先给出上述问题的结论,虽然减重药物改善了体重、血脂、血压、血糖等多种心血管疾病的危险因素,但并不是每一种减重药物都能带来心血管获益。最典型的莫过于西布曲明,早在上市之初,就有人指出服用西布曲明后,患者心血管事件死亡的风险增加。2010年在《新英格兰医学杂志》发表的SCOUT研究结果显示:西布曲明会显著增加中风和心肌梗死的风险。同一年FDA召开了咨询委员会会议,最终的投票结果要求将西布曲明撤市。2012年,FDA颁布“减重药物的心血管风险评估要求”。2015年,欧洲药品管理局(EMA)提出了类似的建议。自此,心血管结局研究(Cardiovascular Outcomes Trials, CVOT)成为减重药物上市的必备研究。
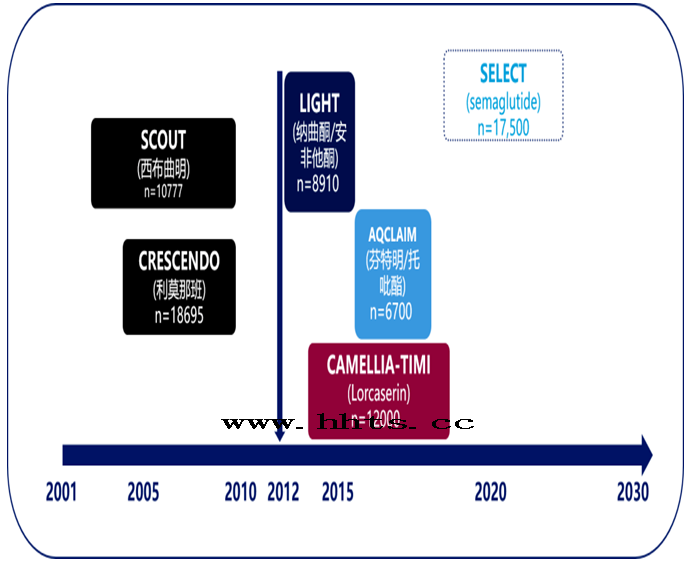
图7表示自2012年以来的减肥药物的CVOT研究
自2012年至今,只有氯卡色林的CAMELLIA-TIMI61是唯一完成的CVOT研究。但其结果为非劣效达成,且基于对氯卡色林CVOT结果的分析发现,氯卡色林组肿瘤发生率更高(7.7% vs 7.1%),并有聚集倾向。权衡风险大于潜在获益,FDA于2020年1月要求其从美国市场撤市。基于以上结果,是否可以得出结论--减重药物对心血管风险毫无改善呢?在糖尿病领域有卓越降糖和减重疗效的GLP-1RA,近年来给我们带来了一丝曙光。在LEADER试验中,1.8 mg利拉鲁肽可降低2型糖尿病患者的心血管事件风险,这被监管机构作为证据支持3.0 mg利拉鲁肽的心血管安全性(注:利拉鲁肽3.0mg尚未在中国上市,利拉鲁肽的临床使用请参考中国说明书) 20。一项对7项在2型糖尿病患者中进行的GLP-1RA CVOT研究数据进行的荟萃分析显示 21 :GLP-1RA 可显著降低2型糖尿病合并CVD或CV高风险患者的MACE风险,这些研究中患者的基线平均BMI>30 kg/m 2。基于此,GLP-1RA近年来在肥胖/超重人群中进行了多项临床试验研究。如果未来GLP-1RA被证实在肥胖/超重患者的CVOT研究中,可以降低MACE风险,带来心血管获益,那么很可能被指南所推荐。
总 结:肥胖及其并发症形成的症候群,与心血管疾病密切相关。减重治疗可以改善心血管疾病风险因素。对生活方式干预的Look AHEAD研究事后分析以及减重手术的SOS研究均显示:体重减轻能带来部分心血管获益。尽管减肥药物的临床研究显示可以改善心血管的危险因素,但是截至目前还没有减肥药物在CVOT研究中被证实其心血管安全性优于安慰剂。